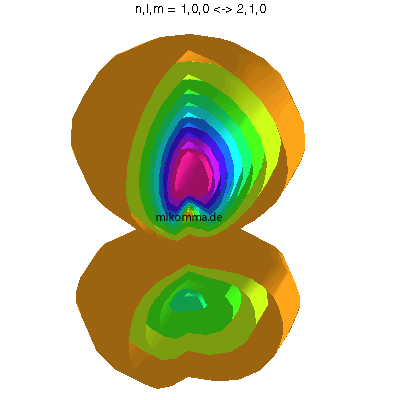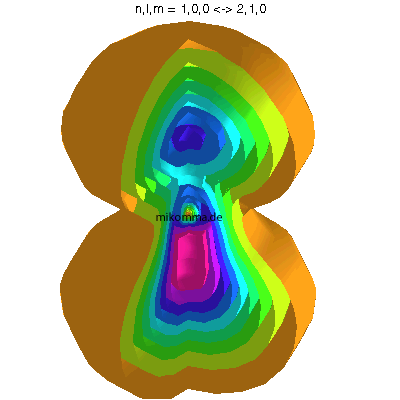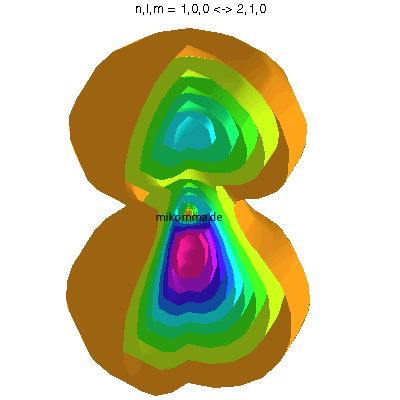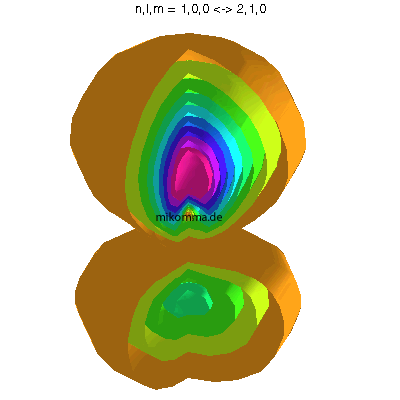Durch Emission oder Absorption von elektromagnetischer Strahlung.
In der Quantenphysik berechnet man den Übergang von einem zum anderen
Zustand durch die Überlagerung von Zuständen, z.B. mit den genannten
Quantenzahlen, zu denen auch bestimmte Frequenzen gehören. Das Ergebnis
ist eine Schwingung mit der Differenz der Frequenzen.
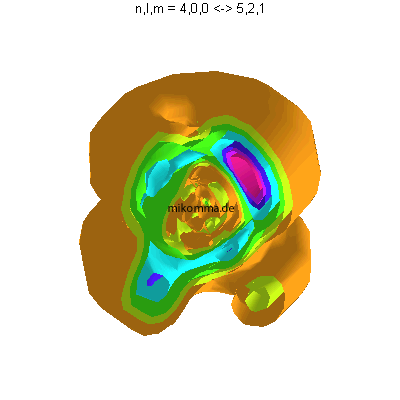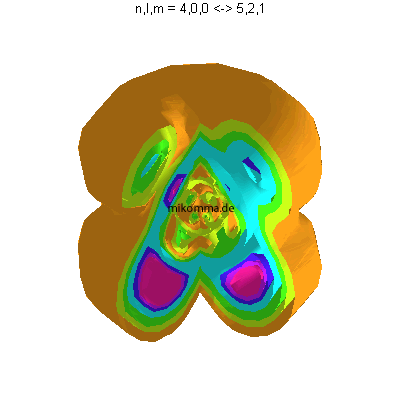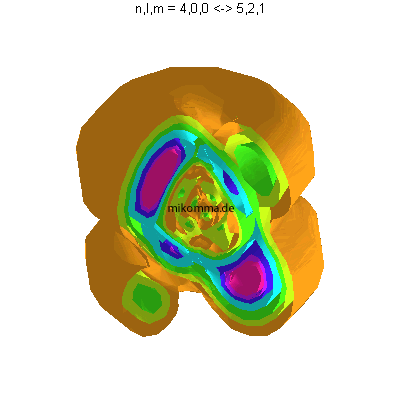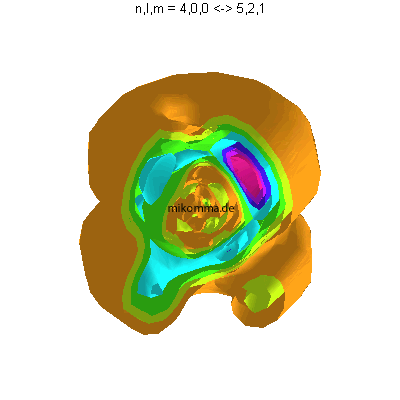
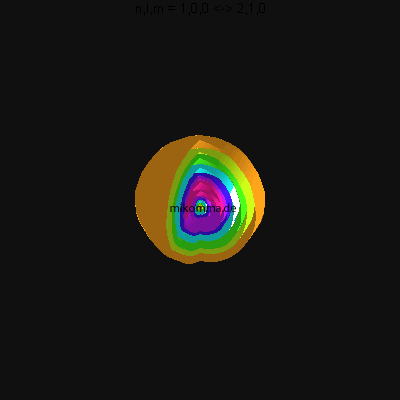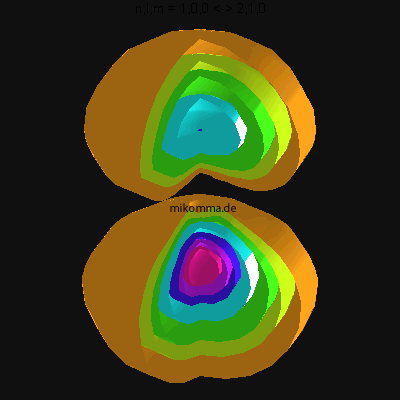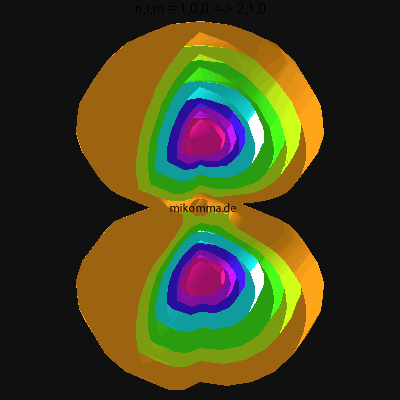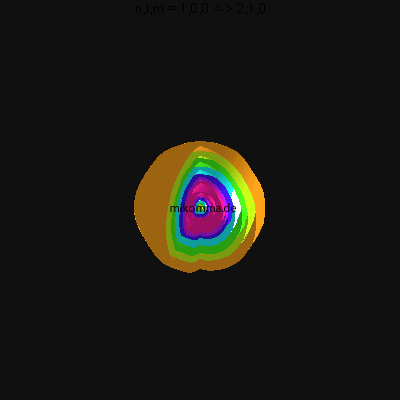
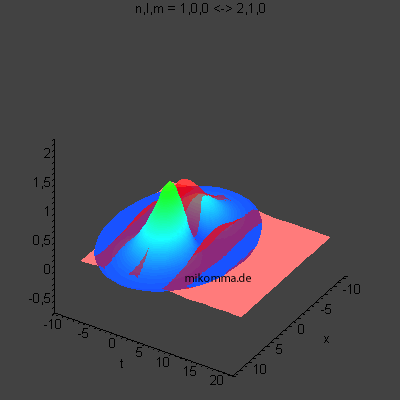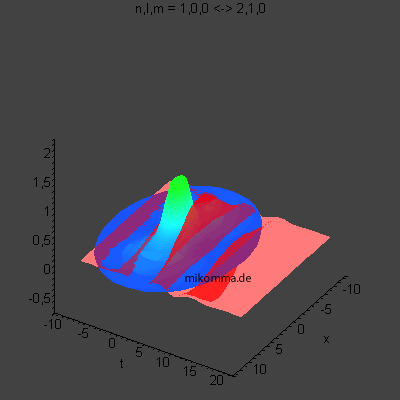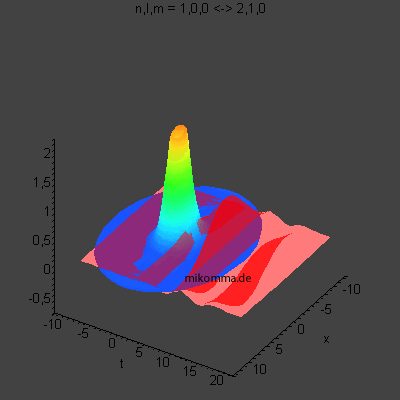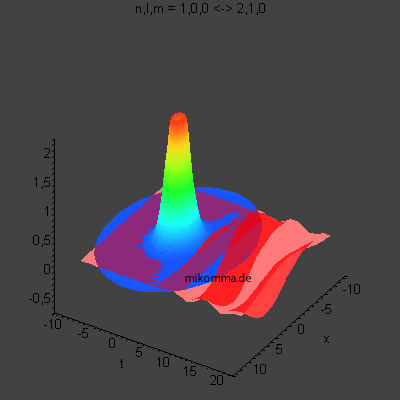
In der Animation sind neun Flächen gleicher Dichte der Elektronenladung
(oder in der Sprache der Quantenphysik der Aufenthaltswahrscheinlichkeit
des Elektrons) dargestellt, von violett (hohe
Aufenthaltswahrscheinlichkeit) bis orange.
Das Atom führt eine Dipolschwingung aus (in der Mitte ist der positiv
geladene Kern zu denken) und gibt deshalb Dipolstrahlung ab oder
absorbiert sie.
Für Licht beträgt die Frequenz der Schwingung etwa 10^14Hz. Der
Vorgang/Übergang kann bis zu einigen Nanosekunden dauern, also etwa
100000 Schwingungen - je Lebensdauer des angeregten Zustands.
Und wo ist nun der Quantensprung geblieben?